في صباح خريفي من نوفمبر 2014، وقف اقتصادي من بوسطن اسمه جوزيف ديماسي أمام حشد من الصحفيين والباحثين ليعلن رقماً واحداً. لم يكن يعلم أن هذا الرقم سيتحول خلال أسابيع إلى أقوى سلاح سياسي في ترسانة صناعة الأدوية: 2.558 مليار دولار. هذا، وفقاً لمركز تافتس لدراسة تطوير الأدوية، هو ما يكلفه إيصال دواء واحد جديد من المختبر إلى يد المريض.[1]
انتشر الرقم كالنار في الهشيم. تلقفته غرف الأخبار وقاعات الكونغرس وأروقة منظمة الصحة العالمية. صار يُستدعى في كل نقاش حول تسعير الأدوية كأنه بديهية لا تقبل الجدل. والمفارقة أنه نُشر للعالم قبل عامين كاملين من خضوعه لمراجعة الأقران الأكاديمية في دورية علمية محكّمة.[2]
لكن ما لم تذكره العناوين الصحفية هو أن باحثين مستقلين، يستخدمون بيانات عامة يمكن لأي شخص التحقق منها، توصلوا إلى أرقام مختلفة جداً. 648 مليون دولار وفقاً لدراسة في JAMA Internal Medicine.[3] 985 مليون دولار وفقاً لدراسة في JAMA.[4] 879 مليون دولار وفقاً لدراسة كلّفتها وزارة الصحة الأمريكية نفسها.[5] فجوة تبلغ مئات الملايين بين ما تقوله الصناعة وما تقوله الأدلة المستقلة. وهذه الفجوة ليست مجرد خلاف أكاديمي حول منهجية البحث. إنها صراع مباشر على السردية التي تحكم أسعار الأدوية، وتحدد من يحيا ومن يموت لأنه لا يستطيع تحمّل ثمن العلاج.
هذا التحقيق يدخل إلى داخل الرقم، يفككه قطعة قطعة: كيف يُحسب، ولماذا يتضخم، وأين تذهب الأموال فعلاً في كل مرحلة من مراحل تطوير الدواء. والأهم: هل تبرر هذه التكاليف الأسعار التي يدفعها المرضى، أم أنها بنية محاسبية صُممت لخدمة أرباح المساهمين أكثر من خدمة العلم؟
ما وراء الرقم: كيف تصنع ملياري دولار من 1.4 مليار
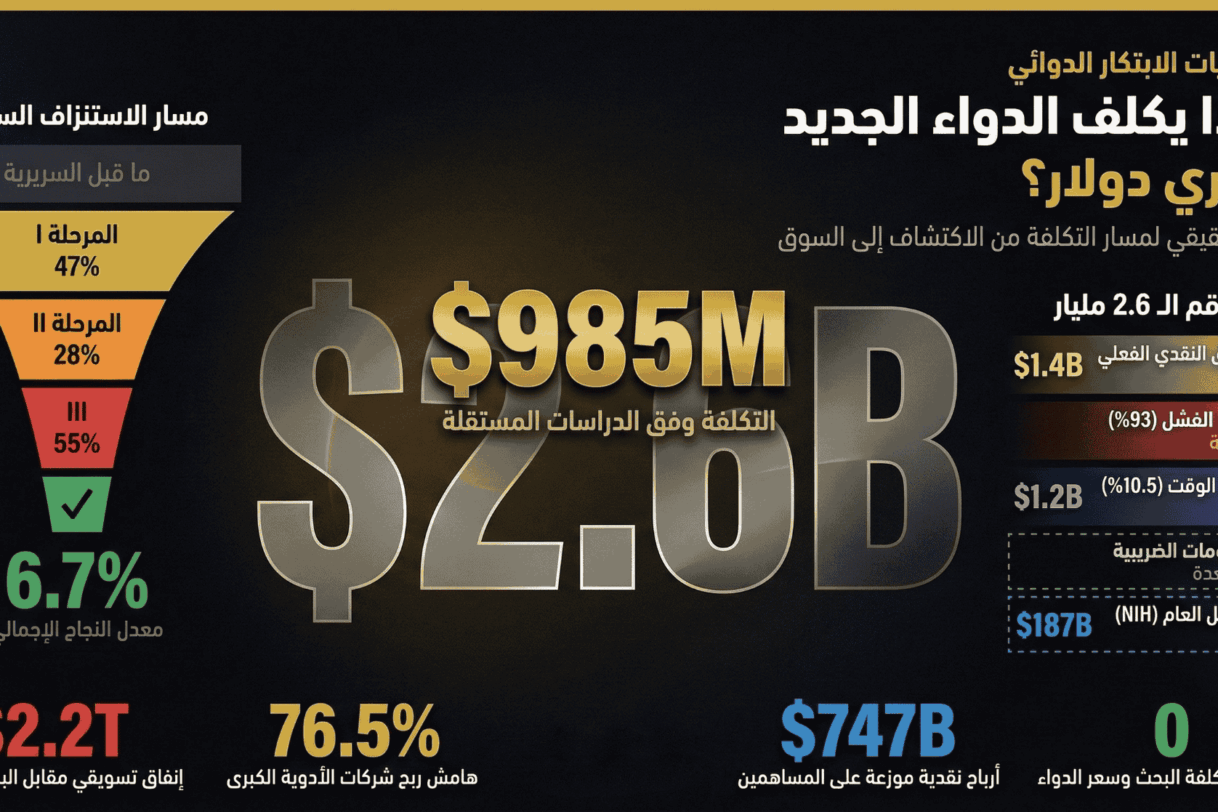
لنبدأ بحقيقة لا يذكرها أحد في العناوين: نصف رقم الـ 2.6 مليار دولار ليس إنفاقاً حقيقياً. التقدير الذي نشره ديماسي وغرابوسكي وهانسن في مجلة Journal of Health Economics عام 2016 ينقسم إلى طبقتين مختلفتين تماماً في طبيعتهما.[2]
الطبقة الأولى هي الإنفاق النقدي الفعلي: 1.395 مليار دولار. هذا هو المال الذي خرج حرفياً من خزائن الشركات ودُفع لباحثين ومستشفيات ومختبرات وموردين. يتضمن هذا الرقم تكلفة جميع الأدوية التي فشلت في الطريق، موزعة حسابياً على الأدوية التي نجحت. وهو رقم مرتفع بلا شك، لكنه ليس الرقم الذي تصدّر العناوين.[6]
الطبقة الثانية هي “تكلفة رأس المال”: 1.163 مليار دولار. وهذا ليس مالاً أُنفق بل مالاً كان يمكن أن يُجنى لو استثمرت الشركة أموالها في أدوات مالية أخرى بدلاً من البحث الدوائي خلال السنوات العشر إلى الخمس عشرة التي يستغرقها التطوير. استخدمت الدراسة معدل خصم سنوي قدره 10.5%، وهو ما يعني أن كل دولار يُستثمر في بداية المسار يتضاعف تقريباً بحلول لحظة الموافقة.[2] هذا العنصر الواحد يضيف نحو 45% إلى الرقم النهائي. أضف إلى ذلك 312 مليون دولار لأبحاث ما بعد الموافقة، ويصل الإجمالي إلى 2.87 مليار عبر دورة حياة الدواء الكاملة.[7]
ولعل الأمر الأكثر إثارة للقلق هو أن هذه الدراسة بُنيت على بيانات سرية قدّمتها عشر شركات لم يُكشف عن هوياتها، حول 106 أدوية لم يُكشف عن أسمائها، دخلت التجارب السريرية بين 1995 و2007. لا يمكن لأي باحث مستقل في العالم مراجعة هذه البيانات أو التحقق منها.[8] وحين كتب جيري أفورن من كلية الطب بجامعة هارفارد عن الدراسة في New England Journal of Medicine، طالب بما وصفه بـ “محاسبة أوسع قاعدة وأكثر شفافية”.[9]
رحلة العقد ونصف: أين يذهب كل دولار
لفهم لماذا يكلف تطوير الدواء هذا القدر من المال حتى بأكثر التقديرات تحفظاً، يجب أن نتتبع الرحلة بأكملها. من المختبر إلى الصيدلية، يمر الدواء بأربع مراحل سريرية رئيسية تمتد في المتوسط من عشر إلى خمس عشرة سنة. كل مرحلة تبتلع أموالاً، وكل فشل يُحمّل على كاهل الدواء الذي ينجح في النهاية.
ما قبل السريرية: البحث عن إبرة في كومة جزيئات
قبل أن يُعطى أي مركّب لإنسان، يقضي سنوات في المختبر. تبدأ العملية بفهم البيولوجيا الجزيئية للمرض وتحديد هدف بيولوجي، ثم فحص آلاف المركبات بحثاً عن واحد يتفاعل مع هذا الهدف دون سمية مفرطة. تستهلك هذه المرحلة نحو 31% من إجمالي التكاليف النقدية المباشرة، وتتراوح تكلفتها بين 15 و100 مليون دولار على مدى ثلاث إلى ست سنوات.[10] لكن هنا تظهر ثغرة مهمة في دراسة تافتس: تقديرات تكاليف هذه المرحلة لم تُبنَ على بيانات مشاريع فعلية، بل استُنتجت من نسبة الإنفاق الإجمالي للشركات على البحث والتطوير.[11] بمعنى آخر: أكبر مكوّن تكلفة منفرد في الدراسة هو في جوهره افتراض حسابي وليس قياساً ميدانياً.
المرحلة الأولى: 136 ألف دولار لكل متطوع
حين ينتقل المركّب إلى الاختبار البشري لأول مرة، يكون التركيز على الأمان لا الفعالية. تُجرى التجارب على 15 إلى 100 متطوع، أغلبهم أصحاء، تحت مراقبة طبية مكثفة على مدار الساعة. التكلفة الإجمالية تتراوح بين 4 ملايين و25 مليون دولار، لكن التكلفة لكل مريض مشارك تبلغ 136,783 دولاراً، وهي الأعلى بين جميع المراحل.[12] وفي أحدث بيانات Citeline/Norstella لعام 2024، لا ينجح في تجاوز هذه المرحلة سوى 47% من الأدوية.[13]
المرحلة الثانية: حيث تُصنع الشركة أو تنكسر
في هذه المرحلة يُختبر الدواء لأول مرة على مرضى حقيقيين، بأعداد تتراوح بين 70 و300، بحثاً عن دليل أولي على الفعالية وتحديد الجرعة المثلى. تتراوح التكلفة بين 7 ملايين و92 مليون دولار.[14] وتحمل هذه المرحلة لقب “عنق الزجاجة” لسبب وجيه: 28% فقط من الأدوية تنجح في تجاوزها.[13] معظم الأموال المستثمرة هنا تتبخر في مشاريع لن ترى النور أبداً، ولهذا يعتبرها كثير من المستثمرين المحطة التي تصنع فيها شركة الأدوية الناشئة مستقبلها أو تنهار.
المرحلة الثالثة: المحرك الأكبر للإنفاق
هنا يُنفق الجزء الأعظم من المال. تجارب محورية تشمل مئات إلى آلاف المرضى، موزعين على عشرات المراكز الطبية في دول متعددة. التكلفة تتراوح بين 20 مليوناً و350 مليون دولار لكل تجربة، مع تكلفة 113,030 دولاراً لكل مريض.[12] ونسبة النجاح هنا 55% تقريباً، مع مدة متوسطة تبلغ 31 شهراً.
لكن هذه المتوسطات تخفي تبايناً هائلاً. فوسيط تكلفة تطوير أدوية الأورام يبلغ 2.77 مليار دولار مقابل 766 مليون فقط لأدوية الجهاز العصبي.[4] أما العلاجات الجينية فتصل تكلفتها إلى 5 مليارات دولار تقريباً لكل منتج معتمد.[15] أي رقم متوسط واحد يحجب أكثر مما يكشف. وحتى بعد اجتياز كل هذه المراحل، تبلغ رسوم مراجعة طلب الموافقة وحدها 4.31 مليون دولار في 2025 وترتفع إلى 4.68 مليون في 2026 بموجب قانون PDUFA، وهي رسوم غير قابلة للاسترداد حتى لو رُفض الطلب.[16]
ضريبة الفشل: الحقيقة التي لا يحب أحد الحديث عنها
إذا سألت لماذا تكلف الأدوية كل هذا المال، فالإجابة الأصدق ليست في تكلفة الدواء الناجح، بل في تكلفة كل الأدوية التي فشلت قبله. الاحتمال الإجمالي لنجاح دواء يبدأ المرحلة الأولى في الوصول إلى الموافقة انخفض إلى 6.7% فقط وفقاً لأحدث البيانات الصناعية.[13] هذا يعني أن مقابل كل دواء يصل إلى يد المريض، يفشل نحو أربعة عشر مركّباً في مراحل مختلفة، ويتحمل الدواء الناجح تكاليفها جميعاً.
والمأساة أن الفشل يزداد ثمناً كلما تأخر. فشل مركّب في المختبر يكلف بضعة ملايين. فشل دواء في المرحلة الثالثة بعد سنوات من الاستثمار يكلف مئات الملايين وقد يهدد بقاء الشركة ذاتها.[17] وتتفاوت احتمالات النجاح بشكل مذهل بين التخصصات: أدوية الأورام لا تنجح بنسبة تتجاوز 3.1%، بينما سجلت أدوية الزهايمر معدل فشل كارثياً بلغ 99.6% بين 2002 و2012.[18]
دراسة سيرتكايا التي كلّفتها وزارة الصحة الأمريكية توضح هذا التدرج بأرقام نظيفة: متوسط التكلفة النقدية لكل دواء فردي يبلغ 173 مليون دولار. أضف تكاليف الأدوية الفاشلة يصبح 516 مليوناً. أضف تكلفة الوقت يصبح 879 مليوناً.[5] ثلاث طبقات متراكمة: التكلفة الفعلية، ثم ضريبة الفشل، ثم ضريبة الوقت.
معدل الخصم: حكم قيمي يتنكر في ثوب محاسبي
لو كان في هذه القصة بأكملها قرار واحد يغيّر كل شيء، فهو اختيار معدل الخصم. استخدمت دراسة تافتس معدل 10.5% سنوياً، مشتقاً من نموذج تسعير الأصول الرأسمالية لأسهم شركات الأدوية. هذا المعدل يعكس ما يتوقعه المساهم من عائد على استثماره في صناعة عالية المخاطر.[2]
لكن السؤال هو: لماذا نحسب تكلفة الدواء من وجهة نظر المساهم وليس من وجهة نظر المريض؟ الحكومة الأمريكية تستخدم معدل 3% في تحليلات التكلفة والعائد.[19] واقترح لايت واربورتون استخدام معدل صفر، بحجة أن شركات الأدوية غالباً ما تموّل أبحاثها من أرباحها المحتجزة لا من اقتراض خارجي.[20]
الفارق العملي مذهل: بمعدل 3%، ينخفض رقم تافتس إلى نحو 1.7 مليار. بمعدل صفر، يصبح 1.4 مليار. المعدل “الصحيح” يعتمد حصراً على من نسأل: المساهم أم المريض. وهذا يجعل ما يُقدّم كحقيقة محاسبية هو في جوهره حكم قيمي متنكر في ثوب رقمي.
ثلاث دراسات قلبت الطاولة
لم تصمد دراسة تافتس طويلاً دون منازع. فقد تعاقبت دراسات مستقلة تستخدم بيانات عامة قابلة للتحقق، وجاءت جميعها بأرقام أقل. الأولى والأكثر أناقة منهجياً جاءت من فيناي براساد وشام مايلانكودي عام 2017 في JAMA Internal Medicine. بدلاً من بيانات سرية، استخدما الإفصاحات المالية العلنية لعشر شركات تقنية حيوية صغيرة لم يكن لديها أي دواء معتمد سابقاً. لأن هذه الشركات لا تمتلك منتجات أخرى، فإن إجمالي إنفاقها يمثل بالضرورة التكلفة الكاملة لبرامجها، بما فيها كل ما فشل. النتيجة: وسيط 648 مليون دولار. لكن الرقم الأهم كان رقم الإيرادات: 67 مليار دولار مقابل إنفاق بحثي بلغ 7.2 مليار فقط. العائد تجاوز التكلفة بأكثر من تسعة أضعاف.[3]
الثانية جاءت من أوليفييه وترز وزملائه في JAMA عام 2020، بتحليل 63 دواءً حصلت على موافقة FDA بين 2009 و2018. وجدوا وسيطاً رأسمالياً يبلغ 985 مليون دولار ومتوسطاً حسابياً يبلغ 1.336 مليار.[4]
والثالثة صدرت عن سيرتكايا وزملائه عام 2024 بتكليف من وزارة الصحة الأمريكية نفسها، ووجدت تكلفة رأسمالية تبلغ 879 مليون دولار.[5]
مقارنة بين التقديرات الرئيسية
| الدراسة | التكلفة الرأسمالية | مصدر البيانات | حجم العينة | الفترة |
| تافتس (DiMasi 2016) | $2.558 مليار | سرية (10 شركات) | 106 أدوية | 1995–2007 |
| Wouters 2020 | $985 مليون | عامة (47 شركة) | 63 دواءً | 2009–2018 |
| Prasad 2017 | $757 مليون | عامة (SEC) | 10 أدوية | 2006–2015 |
| Sertkaya 2024 | $879 مليون | بيانات HHS | شاملة | 2000–2018 |
النمط واضح: التقديرات المستقلة تتجمع حول نطاق 700 مليون إلى 1.3 مليار دولار، أي ما بين ثلث ونصف رقم تافتس. وكلما كانت البيانات عامة وقابلة للتحقق، جاء الرقم أقل.
ست ثغرات في الجدار
ليس النقد الموجه لدراسة تافتس مجرد اعتراض على الأرقام. إنه تفكيك منهجي لبنية الدراسة بأكملها.
أولاً: البيانات سرية ولا يمكن التحقق منها. عشر شركات مجهولة الهوية قدّمت أرقاماً طوعية، وأشار جيمس لوف من منظمة Knowledge Ecology International إلى أن الشركات قد تكون اختارت تقديم بيانات أغلى أدويتها فحسب.[10]
ثانياً: العينة اقتصرت على أدوية طُوّرت بالكامل داخل الشركات الكبرى، متجاهلة المركّبات المرخّصة من جامعات أو شركات صغيرة، وهي تمثل شريحة متنامية من الأدوية المعتمدة.[21]
ثالثاً: الدراسة تتجاهل تماماً الخصومات الضريبية. في الولايات المتحدة، تسترد الشركات ما يصل إلى 50% من تكاليف التجارب السريرية للأدوية اليتيمة كائتمانات ضريبية. وبعد حساب هذه الخصومات، قدّرت منظمة Public Citizen التكلفة الفعلية بنحو 90 مليون دولار فقط.[21]
رابعاً: أعلنت منظمة أطباء بلا حدود أن الرقم “غير موثوق”. وقال مدير سياساتها روهيت مالباني: “إذا صدّقت هذا الرقم، فأنت على الأرجح تصدّق أيضاً أن الأرض مسطحة”. واستشهدت المنظمة بتطويرها أدوية للأمراض المهملة بتكاليف تتراوح بين 50 و186 مليون دولار شاملة الفشل. وفي 2024، نشرت التكاليف الكاملة لتجربتها السريرية TB-PRACTECAL للسل بمبلغ 36 إلى 45 مليون دولار، في سابقة هي الأولى من نوعها.[22][23]
خامساً: مركز تافتس نفسه يتلقى نحو 55% من ميزانيته التشغيلية من شركات الأدوية، وهو ما يثير تساؤلات مشروعة حول استقلالية النتائج التي تخدم مباشرة مصالح الممولين.[24]
سادساً: تتجاهل الدراسة تماماً المساهمة العامة في اكتشاف الأدوية. والأرقام هنا مذهلة.
الجمهور يدفع مرتين
وجدت دراسة كليري وزملائه عام 2018 في PNAS أن تمويل المعاهد الوطنية للصحة الأمريكية (NIH) ساهم في الأبحاث المنشورة المرتبطة بـ كل واحد من الأدوية الـ 210 التي وافقت عليها FDA بين 2010 و2016. إجمالي التمويل: أكثر من 100 مليار دولار عبر أكثر من 200,000 سنة من المنح البحثية.[25] وفي تحليل موسّع عام 2023، وُجد أن NIH استثمرت 187 مليار دولار في أبحاث مرتبطة بـ 356 دواءً معتمداً، بمعدل 1.44 مليار لكل دواء أول في فئته، وهو رقم لا يقل عن استثمار الصناعة ذاتها.[26]
لقاحات كوفيد بتقنية mRNA تقدم المثال الأوضح. تجاوز الاستثمار العام الأمريكي فيها 31.9 مليار دولار حتى مارس 2022، شاملاً عقوداً من أبحاث NIH ومنح DARPA وعقود عملية Warp Speed التي أزالت كل أنواع المخاطر: العلمية والتنظيمية والتصنيعية والسوقية. ومع ذلك، جنت شركة موديرنا وحدها عشرات المليارات.[27] الجمهور إذن يدفع مرتين: مرة بالضرائب التي تموّل الاكتشاف، ومرة بالأسعار المرتفعة حين يشتري الدواء.
حين يتنكر التسويق بلباس العلم
ثمة جانب مظلم في حسابات البحث والتطوير نادراً ما يُناقش. “تجارب الاستزراع” (Seeding Trials) هي دراسات سريرية تُجرى بعد الموافقة على الدواء، هدفها المعلن علمي لكن غرضها الحقيقي تسويقي: تعويد الأطباء على وصف الدواء من خلال جعلهم “باحثين مشاركين”.[28]
في قضية دواء فيوكس (Vioxx)، كشفت وثائق داخلية لشركة ميرك أن تجربة ADVANTAGE صُممت من قبل قسم التسويق لا البحث العلمي. هذه الممارسات تظهر في الميزانيات كإنفاق على “البحث والتطوير”، مما يضخم الأرقام التي تُوظّف لاحقاً لتبرير الأسعار المرتفعة.[28]
الذكاء الاصطناعي: وعد كبير وأثر صغير حتى الآن
أبرز حالة هي دواء رنتوسيرتيب (Rentosertib) من شركة Insilico Medicine: حُدد الهدف البيولوجي والجزيء الدوائي معاً باستخدام الذكاء الاصطناعي التوليدي، وأُنجزت مرحلة الاكتشاف في 18 شهراً بتكلفة 150 ألف دولار فقط، مقابل سنتين ونصف إلى أربع سنوات للمتوسط الصناعي.[29] وفي يونيو 2025، أظهرت نتائج المرحلة الثانية في Nature Medicine تحسناً ملموساً لدى مرضى التليف الرئوي، في أول إثبات سريري لاكتشاف دوائي مدعوم بالذكاء الاصطناعي من البداية إلى النهاية.[30]
لكن التقييم الأمين يقتضي الاعتراف بأن الذكاء الاصطناعي ضغط حتى الآن مرحلة الاكتشاف، وهي الأرخص في المسار. المراحل السريرية الباهظة لم تتأثر بعد. ولم يحصل أي دواء طُوّر بالذكاء الاصطناعي على موافقة كاملة حتى الآن. وكما لاحظ تقرير Deloitte لعام 2025: الذكاء الاصطناعي “لم يُحدث بعد أثراً في مسار المئة شهر من المختبر إلى التسجيل”.[31]
الأرقام التي تفضحها الإفصاحات المالية
إذا كان رقم الـ 2.6 مليار هو الحجة المركزية لتبرير الأسعار المرتفعة، فإن الإفصاحات المالية للشركات ذاتها تقوّضها من الداخل. دراسة في BMJ عام 2023 وجدت أن 15 من أكبر الشركات أنفقت 2.2 تريليون دولار على التسويق والمصاريف الإدارية مقابل 1.4 تريليون على البحث بين 1999 و2018. الإنفاق التسويقي تجاوز البحثي بنسبة 57%.[32] وأنفقت 14 شركة كبرى 747 مليار دولار على إعادة شراء أسهمها وتوزيعات الأرباح بين 2012 و2021، متجاوزة ما استثمرته في البحث بنسبة 13%.[33]
هوامش الربح تؤكد الصورة. وجدت دراسة في JAMA أن هامش الربح الإجمالي لشركات الأدوية بلغ 76.5% مقابل 37.4% لبقية شركات S&P 500. ومتوسط صافي الربح 23.2% سنوياً، عشرة أضعاف قطاعات سلسلة توريد الأدوية الأخرى.[34][35]
وتقدم قصة هيوميرا (Humira) النموذج الأكثر فجاجة. أكثر من 200 مليار دولار إيرادات تراكمية مقابل 5.2 مليار استثمار بحثي، أي أن البحث لم يمثل سوى 7.4% من الإيرادات الأمريكية. وحين قدّمت AbbVie أكثر من 250 طلب براءة اختراع (90% منها بعد الموافقة الأصلية)، أنشأت “غابة براءات” أخّرت البدائل الحيوية سبع سنوات. وحين دخلت هذه البدائل سوق هولندا أخيراً، انخفضت الأسعار 90%.[36]
والأكثر دلالة: دراسة في JAMA Network Open عام 2022 لم تجد أي ارتباط إحصائي بين حجم الاستثمار البحثي وأسعار إطلاق الأدوية.[37] الشركات لا تسعّر بناءً على ما أنفقته، بل بناءً على أقصى ما يتحمله السوق. وتحليل RAND لعام 2024 يؤكد أن أسعار الأدوية الأمريكية تبلغ 2.78 ضعف المتوسط في 33 دولة، وترتفع إلى 4.22 ضعف للأدوية ذات العلامة التجارية.[38] الجزيئات ذاتها تُباع بأسعار أقل بكثير في دول تفاوض على الأسعار دون أن ينهار فيها الابتكار.
نموذج بديل يثبت أن الابتكار ممكن بأقل
تقدم مبادرة أدوية الأمراض المهملة (DNDi) الدليل العملي. تكلفة تطوير كيان كيميائي جديد عبرها تتراوح بين 60 و190 مليون يورو شاملة تكاليف الفشل، بينما تنخفض تكلفة إعادة استخدام أدوية حالية إلى 4 إلى 32 مليون يورو فقط.[39] تعتمد المبادرة على فك الارتباط بين تكلفة البحث وسعر المنتج، مما يثبت أن جزءاً كبيراً من الـ 2.6 مليار هو نتاج للبنية الرأسمالية لا للضرورة العلمية.[40]
خاتمة: صراع على القيمة لا مسألة حسابية
التكلفة الحقيقية لتطوير دواء جديد لا تبلغ 2.6 مليار دولار ولا 43 مليوناً. التقديرات المستقلة الأكثر مصداقية تتجمع حول 700 مليون إلى 1.3 مليار دولار حين نشمل تكاليف الفشل ونستخدم معدل خصم معقول. رقم تافتس مضخّم بمعدل خصم مرتفع، وعينة منحازة، وافتراضات غير مرتبطة ببيانات فعلية، وتجاهل كامل للإعانات الضريبية والمساهمات البحثية العامة.
تطوير الأدوية عملية مكلفة ومحفوفة بالمخاطر فعلاً. البيولوجيا البشرية معقدة، والفشل حقيقي، وضريبة الاستنزاف باهظة. لكن شركات تنفق على إعادة شراء أسهمها أكثر مما تنفق على البحث، وتحقق هوامش ربح ثلاثة أضعاف متوسط الشركات الكبرى، وتسعّر أدويتها بأربعة أضعاف الأسعار الدولية، لا تستطيع أن تدّعي بمصداقية أن الأسعار المرتفعة هي ببساطة ثمن الابتكار.
لغز الملياري دولار هو في جوهره صراع على القيمة: من يتحمل تكلفة الابتكار، ومن يجني ثماره، ومن يُحرم منه. هذا الصراع سيحدد ملامح العدالة الصحية في القرن الحادي والعشرين.
في الجزء الثاني من هذه السلسلة
ناقشنا في هذا الجزء تكاليف تطوير الأدوية الكيميائية التقليدية. لكن صناعة الأدوية تشهد تحولاً جذرياً نحو المنتجات البيولوجية والعلاجات الخلوية والجينية: أدوية تُنتجها خلايا حية، وعلاجات تكلف جرعتها الواحدة أكثر من نصف مليون دولار تصنيعاً وحده. في الجزء الثاني، نستكشف كيف تختلف اقتصاديات هذا العالم الجديد، ولماذا حصلت شركة على ثلاث موافقات تنظيمية ثم بيعت بـ 29 مليون دولار فقط.
المراجع
[1] Tufts Center for the Study of Drug Development. Media briefing, November 18, 2014. “Cost to Develop and Win Marketing Approval for a New Drug Is $2.6 Billion.”
[2] DiMasi JA, Grabowski HG, Hansen RW. “Innovation in the pharmaceutical industry: New estimates of R&D costs.” Journal of Health Economics, 47:20–33, 2016.
[3] Prasad V, Mailankody S. “Research and Development Spending to Bring a Single Cancer Drug to Market and Revenues After Approval.” JAMA Internal Medicine, 177(11):1569–1575, 2017.
[4] Wouters OJ, McKee M, Luyten J. “Estimated Research and Development Investment Needed to Bring a New Medicine to Market, 2009–2018.” JAMA, 323(9):844–853, 2020.
[5] Sertkaya A, et al. “Costs of Drug Development and Research and Development Intensity in the US, 2000–2018.” JAMA Network Open, 7(6):e2415445, 2024.
[6] Bioanalysis Zone. “New study claims that cost to develop new drug is $2.6 billion.” 2014.
[7] Applied Clinical Trials Online. “Tufts Center for the Study of Drug Development — Cost of Developing New Drugs.”
[8] KEI. “KEI comment on the new Tufts Study on Drug Development Costs.” Knowledge Ecology International, 2014.
[9] Avorn J. “The $2.6 Billion Pill — Methodologic and Policy Considerations.” New England Journal of Medicine, 372:1877–1879, 2015.
[10] KEI. “KEI comment on the new Tufts Study on Drug Development Costs.” 2014.
[11] The Incidental Economist. “$2.6 Billion to Develop a Drug? New Estimate Makes Questionable Assumptions.” 2014.
[12] Abacum. “Clinical Trial Costing: Phase-By-Phase Budget Guide.” 2025.
[13] Norstella/Citeline. “Clinical Development Success Rates 2014–2023.” 2024.
[14] Southern Star Research / ProRelix Research. “Clinical trial costs by phase.” 2025.
[15] Evernorth. “Challenges in bringing gene therapies to market.” 2024.
[16] Federal Register. “Prescription Drug User Fee Rates for Fiscal Year 2025 & 2026.”
[17] Research Solutions. “In Drug Development, Early Failure Breeds Success.” 2024.
[18] Preprints.org. “Pharmaceutical Drug Lifecycle: A Comprehensive Scientific Review.” 2026.
[19] U.S. Government cost-benefit analysis guidelines. Office of Management and Budget, Circular A-4.
[20] Light DW, Warburton R. “Demythologizing the high costs of pharmaceutical research.” BioSocieties, 6:34–50, 2011.
[21] Public Citizen. “Pharmaceutical Research Costs: The Myth of the $2.6 Billion Pill.” 2017.
[22] MSF/Doctors Without Borders. “R&D Cost Estimates: MSF Response to Tufts CSDD Study.” 2014.
[23] MSF. “MSF publishes cost of its TB clinical trial (TB-PRACTECAL).” 2024.
[24] Wikipedia. “Tufts Center for the Study of Drug Development.” (Funding sources.)
[25] Cleary EG, et al. “Contribution of NIH funding to new drug approvals 2010–2016.” PNAS, 115(10):2329–2334, 2018.
[26] Bentley University / JAMA Health Forum. “NIH investment in new drug approvals comparable to pharmaceutical industry.” 2023.
[27] Cross S, et al. “US public investment in development of mRNA covid-19 vaccines.” BMJ, 380:e073747, 2023.
[28] Hill KP, et al. “The ADVANTAGE Seeding Trial: A Review of Internal Documents.” Annals of Internal Medicine, 149(4):251–258, 2008.
[29] Insilico Medicine. “Rentosertib (ISM001-055) discovery and development.” Press releases 2024–2025.
[30] Insilico Medicine. “Nature Medicine Publication of Phase IIa Results of Rentosertib.” June 2025.
[31] Drug Discovery Trends. “From 1.5% to 5.9%: Deloitte explores Big Pharma’s R&D IRR climb.” 2025.
[32] BMJ 2023;380:bmj-2022-071710. “High drug prices are not justified by industry’s spending on research and development.”
[33] Lazonick W, Tulum O. Stock buybacks and dividends analysis, 2012–2021. U.S. House Committee on Oversight, 2021.
[34] Ledley FD, et al. “Profitability of Large Pharmaceutical Companies Compared With Other Large Public Companies.” JAMA, 323(9):834–843, 2020.
[35] CSRxP. “Pharmaceutical Industry’s Profit Margins Still 10 Times Greater Than Other Sectors.” 2024.
[36] U.S. House of Representatives. “Drug Pricing Investigation AbbVie—Humira and Imbruvica Staff Report.” 2021.
[37] PharmaVoice. “Do R&D costs justify the price of drugs? Nope, new study says.” 2023. (JAMA Network Open 2022.)
[38] RAND Corporation. “Prescription Drug Prices in the U.S. Are 2.78 Times Those in Other Countries.” February 2024.
[39] DNDi. “Transparency of R&D costs.” 2024.
[40] Health Policy Watch. “New Research Study Describes DNDi As ‘Commons’ For Public Health.” 2024.